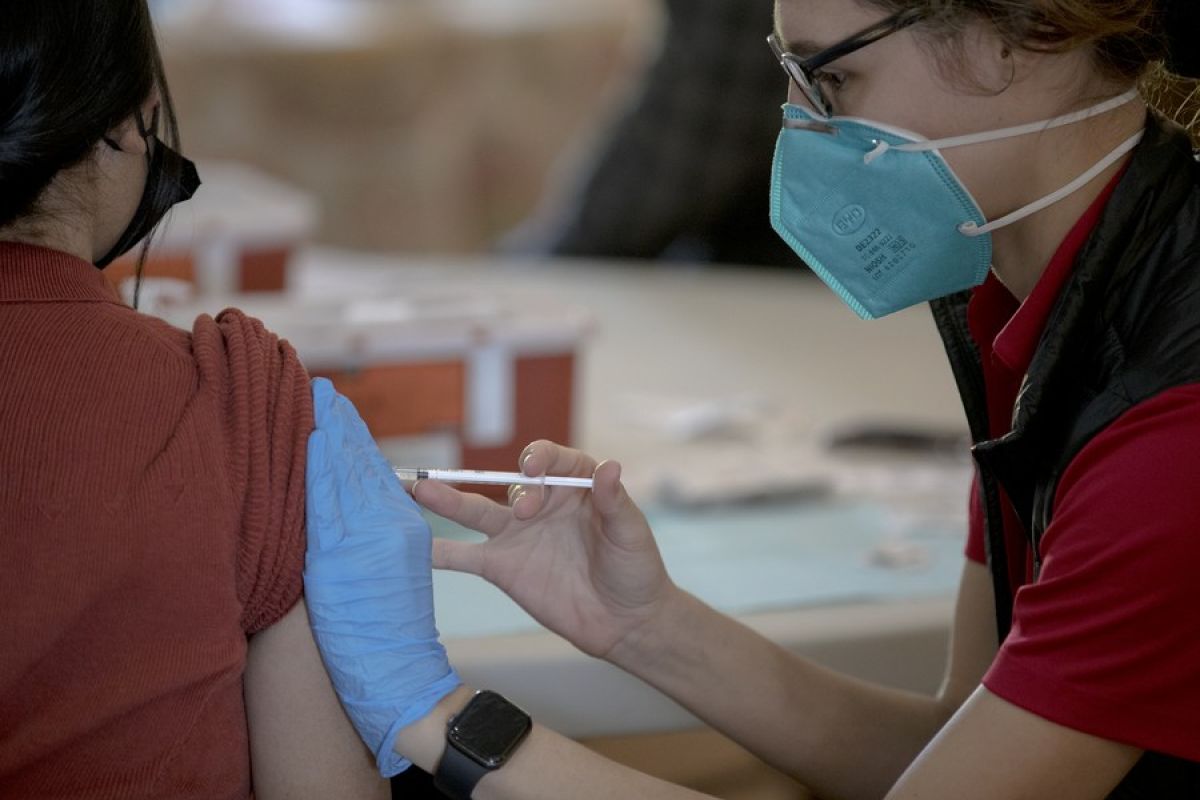
Vaksin Novavax akan tersedia sebagai rangkaian primer dua dosis bagi orang dewasa, dengan interval tiga pekan.
Manfaat yang telah diketahui dan potensial dari vaksin tersebut lebih besar daripada risiko yang diketahui dan potensial bagi orang berusia 18 tahun ke atas, dan vaksin itu kemungkinan efektif dalam mencegah COVID-19, kata FDA dalam sebuah pernyataan.
Vaksin tersebut merupakan vaksin COVID-19 keempat yang tersedia di AS, dan menggunakan jenis teknologi vaksin yang berbeda dari tiga vaksin lain yang telah disetujui sebelumnya.
Menurut FDA, vaksin Novavax mengandung protein lonjakan SARS-CoV-2 dan adjuvan Matrix-M. Adjuvan dimasukkan ke dalam vaksin untuk meningkatkan respons imun dari individu yang divaksinasi.
Vaksin itu dievaluasi dalam sebuah penelitian secara acak, tersamar, dan terkontrol plasebo yang sedang berlangsung di AS dan Meksiko. Secara keseluruhan, vaksin tersebut 90,4 persen efektif dalam mencegah COVID-19 ringan, sedang, atau berat, papar FDA.
Diungkapkan FDA, efek samping yang paling sering dilaporkan dari vaksin itu meliputi rasa nyeri, kemerahan dan bengkak di lokasi suntikan, kelelahan, nyeri otot, sakit kepala, nyeri sendi, mual, dan demam.

"Setelah analisis dan evaluasi data yang komprehensif, dan penilaian proses manufaktur dan informasi, serta masukan dari komite penasihat independen eksternal FDA, para ahli medis dan pakar ilmiah FDA telah menentukan bahwa vaksin tersebut memenuhi standar tinggi FDA dalam hal keamanan dan efektivitas untuk izin penggunaan darurat," sebut Peter Marks, Direktur Pusat Evaluasi dan Penelitian Biologi FDA.
Para penasihat vaksin independen dari Pusat Pengendalian dan Pencegahan Penyakit (Centers for Disease Control and Prevention/CDC) AS akan mempertimbangkan apakah bakal merekomendasikan vaksin tersebut.
Selanjutnya, Direktur CDC akan memutuskan untuk menyetujui rekomendasinya sebelum vaksin Novavax siap diberikan di Negeri Paman Sam.
Komite Penasihat CDC untuk Praktik Imunisasi dijadwalkan akan bertemu pada 19 Juli mendatang.
Pada Senin (11/7), pemerintah AS mengumumkan bahwa pihaknya telah mendapatkan 3,2 juta dosis vaksin Novavax.
Pewarta: Xinhua
Editor: Zita Meirina
Copyright © ANTARA 2022